2025年8月18日,华中科技大学yl23411永利集团官网李一伟教授和刘笔锋教授团队在《Research》期刊发表了题为"Mechanical Cell Reprogramming on Tissue-Mimicking Hydrogel for Cancer Cell Transdifferentiation"的重要研究成果。该论文可以通过此链接查看:https://spj.science.org/doi/10.34133/research.0810。
论文通讯作者是李一伟教授和刘笔锋教授,论文共同第一作者是博士生任雪晴和郑大一附院王亚超副研究员。该研究开发了一种创新的组织力学仿生水凝胶系统,首次实现了纯粹通过力学信号诱导细胞重编程,不仅能够增强成纤维细胞的干性和双向分化潜能,还能促进癌细胞向脂肪细胞转分化,为再生医学和癌症治疗提供了全新的治疗策略。
研究背景
组织基质的力学特性对维持细胞健康和功能至关重要。随着年龄增长,组织基质失去力学完整性,表现出改变的生物物理特性,这与神经退行性疾病和癌症等多种疾病的发生密切相关。虽然科学家们已经认识到基质力学性质的重要性,但是否能够通过模拟健康组织的力学微环境来维持或恢复细胞的健康状态,仍然是一个未解之谜。
传统的细胞重编程主要依赖生化因子或基因编辑技术,但这些方法可能存在脱靶效应或致瘤风险。近年来,虽然有研究表明某些力学信号可以辅助细胞重编程,但缺乏能够同时模拟天然组织粘弹性和非线性弹性特征的材料平台。天然组织基质同时具有粘弹性和非线性弹性两种重要特征,但现有的合成或天然水凝胶主要只能模拟其中一种特性,这种局限性阻碍了对组织力学微环境在维持细胞功能中作用的深入理解。
创新技术突破
该论文应用海藻酸盐-胶原蛋白互穿网络(IPN)水凝胶系统,构建了同时具有非线弹性生物基质和粘弹性生物基质的"组织力学仿生水凝胶"。这种创新设计巧妙地结合了胶原蛋白网络提供的非线性弹性特征和海藻酸盐网络展现的粘弹性剪切变稀行为。通过调节钙离子交联浓度,研究团队能够在保持胶原蛋白和海藻酸盐浓度一致的情况下,精确控制水凝胶的初始储存模量,从而模拟不同年龄组织的力学特性。
研究的最重要发现是细胞能够通过基质重塑实现远程力学相互作用。在组织仿生水凝胶上培养的成纤维细胞表现新的迁移行为模式:细胞首先在水凝胶表面正常伸展,8小时后开始相互迁移并形成间充质细胞聚集体,细胞聚集导致胶原纤维的重新组织和束状结构形成。这种现象仅在粘弹性和非线性弹性互穿水凝胶中出现,且在纯胶原蛋白或海藻酸盐基质上均未观察到,证明了粘弹性和非线性弹性组分协同作用的重要性。
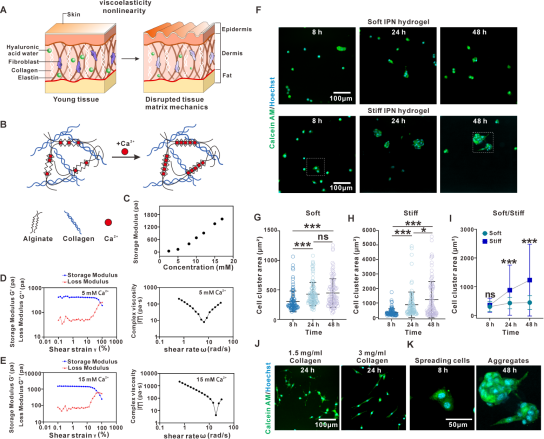
图1.组织仿生水凝胶的构建和间充质聚集体的形成
研究意义和应用前景
该技术在再生医学领域具有广阔的应用前景,可用作患者自体细胞的体外扩增和重编程平台,增强细胞的传代和治疗潜能,也可开发为注射式支架材料,促进组织修复中的细胞聚集和分化。
该研究开发的组织力学仿生水凝胶技术实现纯力学信号诱导的细胞部分重编程。该研究的核心创新在于发现了基质介导的远程细胞-细胞力学相互作用机制,揭示了增强细胞收缩力在重编程过程中的关键作用。这项工作不仅在科学理论上取得了重要进展,更在实际应用中展现了潜力,有望在应对全球老龄化和癌症治疗挑战方面发挥重要作用。
关于研究团队
李一伟教授2020年底从麻省理工学院回国加入华中科技大学任教授,专注于细胞物理力学、类器官智能制造和相分离生物技术开发研究。这项工作得到了国家重点研发计划和国家自然科学基金等项目的支持。团队网站:www.yiweililab.com